Как развести каустическую соду для промывки канализации
Из нашей статьи вы узнаете, как развести каустическую соду для прочистки канализации, что учитывать и в каких трубах применять, меры предосторожности.
Засор канализации на кухне или в ванной комнате – это всегда проблема. Кипяток или вантуз не помогли? Давайте рассмотрим, как выполняется очистка канализационных труб другими способами, в частности, с применением бытовой химии. Например, как прочистить засор в ванной каустической содой.
Причины возникновения засоров канализации
Загрязнения можно разделить на два типа:
- Те, которые можно прочистить каустиком:
- Пучки волос или шерсть животных.
- Пищевые отходы небольшого размера.
- Отложения жира.
- Мелкие косточки и рыбья чешуя.
- Застывшее мыло.
- Для прочистки которых, требуется механическое вмешательство:
- Нерастворимый твердый мусор.
- Грязь после мытья обуви.
- Песок, земля из цветочных горшков.

- Строительные смеси.
- Цементная крошка.
Важно! Каустическая сода (она же «едкий натр», она же «едкая щелочь») относится к веществам, способным нанести вред здоровью. Поэтому обращаться с химикатом следует с особой осторожностью.
Как пользоваться каустической содой для прочистки канализации
Препарат представляет собой мощный природный растворитель органики и нейтрализатор кислоты. Выпускается (и продается) в виде порошка, гранул или чешуек. Для активации твердый состав необходимо растворить в воде.
Важно! Используйте только холодную воду! При контакте с жидкостью, каустическая сода нагревается до 70°C. Если растворять ее горячей водой, возможно закипание, разбрызгивание, термический и химический ожоги.
Как разводить каустическую соду для чистки канализации? Делается это так:
- Пропорции – 1 кг порошка на 3-4 литра воды. Сначала наливается вода (не более чем на 2/3 объема), затем засыпается сода.

- Порошок добавляется частями, с постоянным размешиванием.Важно! При изготовлении раствора следует пользоваться элементарными средствами защиты: защитные очки и резиновые перчатки. В непосредственной близости должен быть источник проточной воды (на случай попадания раствора на кожу).
- Применять каустическую соду для чистки канализации, желательно в горячем виде, она медленно заливается в систему. Если смесь не проходит вся сразу, дождитесь растворения засора, затем вылейте остаток.
- Еще один способ, как использовать каустическую соду для чистки канализации – растворение по месту. Порошок засыпается в сливную трубу, затем заливается вода (в указанной выше пропорции). Методика более агрессивная по отношению к трубам, поэтому использование в пластиковых коммуникациях недопустимо.
Как прочистить канализацию каустической содой для профилактики
Для предупреждения накапливания мусора в трубах, не реже, чем раз в три месяца, канализация проливается щадящим раствором.
Если возникли трудности или опасения, или засор все-таки остался на месте, советуем обратиться к профессионалам, например, в компанию Kanalservis.ru. Специалисты быстро прибудут на место и выполнят всю работу чисто и аккуратно.
Приготовление раствора каустической соды (едкого натра, гидроксида натрия, NaOH)
4 февраля, 2020
В технологических процессах многих предприятий используется раствор едкого натра. Чаще всего закупается готовый раствор гидроксида натрия. В России всего несколько заводов-изготовителей, занимающихся производством каустической соды. Основные – АО «Башкирская содовая компания» (г. Стерлитамак, специализируется на чешуированном едком натре), АО «Каустик» (г. Волгоград, специализируется на гранулированном едком натре).
Все привыкли к тому, что можно купить 46% раствор, а затем разбавить водой до необходимой концентрации. Более концентрированный раствор производители едкого натра не поставляют, т.к. повышается вероятность кристаллизации раствора при понижении температуры, что создаст проблемы при перекачивании. В холодное время года приходится перевозить раствор едкого натра в обогреваемых утепленных танк-контейнерах, что еще больше удорожает и без того недешевую перевозку.
Принимая во внимание еще и:
- монопольно завышенную цену на раствор каустической соды,
- возможные перебои поставок,
- экономию места для хранения раствора
руководство некоторых предприятий задумалось о снижении издержек путем самостоятельного наведения раствора из сухого каустика. Данное решение также позволяет снизить риски, связанные с хранением вещества второго класса опасности. Периодически создавать достаточный запас раствора из сухого реагента проще, чем обеспечивать хранение большого объема агрессивного раствора.
Одно из таких предприятий – ТОО «Cracking Catalyst» (Казахстан, г. Шымкент).
При проработке вопроса приготовления раствора едкого натра технолог предприятия столкнулся со следующими затруднениями:
- При ручном растаривании мешков с гидроксидом натрия неизбежно пыление. Пыль впитывает влагу, образуя вокруг площадки оператора щелочь.
- Растаривать мешки в костюме химзащиты очень затруднительно, неудобно, жарко. Без костюма поражаются открытые кожные покровы оператора. Неясно, как обезопасить персонал.
- При приготовлении щелочи выделяются значительное количество тепла, раствор закипает, возникает обильное щелочное парение.
- За смену нужно успеть растворить 6 900 кг каустической соды (растарить 276 мешков – что весьма трудоемко).
- Ввиду отсутствия соответствующего опыта нет четкого понимания, как самостоятельно изготовить работоспособное оборудование для растворения едкого натра в воде.
Решение проблемы растворения каустической соды
Весной 2018 г ТОО «Cracking Catalyst» обратилось в ООО «Квант Минерал», имеющее опыт изготовления оборудования для безопасного растаривания опасных реагентов и приготовления их растворов.
Уточнив исходные данные заказчика, мы предложили ему для ускорения процесса и снижения трудоемкости операций растаривать едкий натр в биг-бегах (МКР). Получив согласие заказчика, мы разработали под его нужды следующее техническое решение:
Описание технологии растворения
Оператор заполняет исходной водой накопительную емкость.
Контейнеры МКР с каустической содой доставляют автотранспортом в здание узла растворения. С помощью электрического тельфера контейнеры разгружают и устанавливают на площадку.
Оператор закрепляет контейнер на крюк тельфера и с его помощью загружает контейнер в растворный бак (растворитель). Оператор закрывает крышку растворного бака, нажимает кнопку запуска цикла растворения. Растаривание и растворение проводятся в герметично закрытом пространстве, что обеспечивает отсутствие пыления и гарантирует безопасность персонала.
Циркуляционный насос подает воду из накопительной емкости в контейнер МКР с растворяемым веществом. Через перфорированную решетку раствор стекает в нижнюю часть растворителя. Циркуляция раствора продолжается до полного растворения. Цикл растворения и перезагрузки одного контейнера в среднем составляет около 60-90 мин (подбирается при пуско-наладочных работах).
Через перфорированную решетку раствор стекает в нижнюю часть растворителя. Циркуляция раствора продолжается до полного растворения. Цикл растворения и перезагрузки одного контейнера в среднем составляет около 60-90 мин (подбирается при пуско-наладочных работах).
После окончания растворения (время задается таймером) отключается циркуляционный насос и включается сигнализатор окончания цикла. Оператор открывает крышку. Из растворного бака извлекается пустой контейнер.
Готовый раствор каустической соды сливается в имеющиеся у заказчика накопительные емкости.
Для обслуживания оборудования требуется 1 оператор.
Отвод теплоты, образующейся при растворении каустической соды, происходит через пластинчатый теплообменник.
Предусмотренная автоматизация обеспечивает защиту насосов от «сухого хода», автоматическое отключение циркуляционных насосов по завершении цикла растворения, защиту емкостей от перелива, оповещение оператора об аварийных ситуациях, оповещение об окончании растворения. Контроль и управление оборудованием осуществляется при помощи щита управления.
Контроль и управление оборудованием осуществляется при помощи щита управления.
Реализация проекта
После утверждения технического решения и подписания договора, мы приступили к проектированию, комплектации, изготовлению, поставке узла растворения едкого натра.
В ходе реализации проекта заказчик для экономии воды установил градирню – создал закрытый контур охлаждения.
Через 6 месяцев заказчик получил оборудование. В течении 3 последующих недель мы произвели шеф-монтажные и пуско-наладочные работы.
Запас мощности, заложенный в теплообменник, пригодился после окончания работ. Осенью 2018 г в Казахстане установилась жаркая погода и температура исходной воды, подаваемой на охлаждение, увеличилась с 25 °С до 30 °С. Оборудование успешно справилось с повышением нагрузки.
Отзыв ТОО «Cracking Catalyst» на узел растаривания биг-бегов.
Помните: для этого контента требуется JavaScript.Страница не найдена — Портал Продуктов Группы РСС
Сообщите нам свой адрес электронной почты, чтобы подписаться на рассылку новостного бюллетеня.
Мы обрабатываем Ваши данные для того, чтобы отправить Вам информационный бюллетень — основанием для обработки является реализация нашей законодательно обоснованной заинтересованности или законодательно обоснованная заинтересованность третьей стороны – непосредственный маркетинг наших продуктов / продуктов группы PCC .
Как правило, Ваши данные мы будем обрабатывать до окончания нашего с Вами общения или же до момента, пока Вы не выразите свои возражения, либо если правовые нормы будут обязывать нас продолжать обработку этих данных, либо мы будем сохранять их дольше в случае потенциальных претензий, до истечения срока их хранения, регулируемого законом, в частности Гражданским кодексом.
В любое время Вы имеете право:
- выразить возражение против обработки Ваших данных;
- иметь доступ к Вашим данным и востребовать их копии;
- запросить исправление, ограничение обработки или удаление Ваших данных;
- передать Ваши персональные данные, например другому администратору, за исключением тех случаев, если их обработка регулируется законом и находится в интересах администратора;
- подать жалобу Президенту Управления по защите личных данных.
Получателями Ваших данных могут быть компании, которые поддерживают нас в общении с Вами и помогают нам в ведении веб-сайта, внешние консалтинговые компании (такие как юридические, маркетинговые и бухгалтерские) или внешние специалисты в области IT, включая компанию Группы PCC .
Больше о том, как мы обрабатываем Ваши данные Вы можете узнать из нашего Полиса конфиденциальности.
Очистка самогона каустической содой
Как очистить самогон каустической содой
Очистка самогона каустической содой (едким натром) — то же самое, что очистка пищевой содой, или кальцинированной. По сути данная статья призвана развеять заблуждения, возникающие из-за непонимания понятий и процессов, а заодно приоткроем завесу над дозировками. Сразу скажу, что переписываемые на различных сайтах методики по очистке самогона содой, потом марганцовкой, а потом еще каустической содой — бред, извините, сивой кобылы. Это как «масло масляное». Или разводить самогон водой, а потом еще раз водой. Потому что берем мы соду пищевую, кальцинированную, или каустик — разницы никакой — все вышеперечисленное — щелочь, и отличие только в дозировке.
По сути данная статья призвана развеять заблуждения, возникающие из-за непонимания понятий и процессов, а заодно приоткроем завесу над дозировками. Сразу скажу, что переписываемые на различных сайтах методики по очистке самогона содой, потом марганцовкой, а потом еще каустической содой — бред, извините, сивой кобылы. Это как «масло масляное». Или разводить самогон водой, а потом еще раз водой. Потому что берем мы соду пищевую, кальцинированную, или каустик — разницы никакой — все вышеперечисленное — щелочь, и отличие только в дозировке.
Химическая сторона процесса очистки
Давайте, чтобы в дальнейшем не путаться, сразу вспомним школьный курс химии, и расставим все точки над i:
1). NaHCO3 — пищевая сода. Также в обиходе может называться питьевая сода или чайная сода. Если оперировать химическими терминами, то это гидрокарбонат натрия или натрий двууглекислый.
2). Na2CO3 — кальцинированная сода, или же карбонат натрия
3). NaOH — каустическая сода, она же каустик, едкий натр, едкая щёлочь.
NaOH — каустическая сода, она же каустик, едкий натр, едкая щёлочь.
Теперь давайте окунемся в формулы происходящего:
Щелочь в этой реакции нам нужна для нейтрализации кислот, содержащихся в продукте — муравьиной и уксусной. Давайте посмотрим на примере муравьиной кислоты. Возьмем по очереди все три варианта — пищевую соду, кальцинированную и каустическую.
HCOOH + NaHCO3 → HCOONa + h30 + CO2
2HCOOH + NaHCO3 → 2HCOONa + h3O + CO2
HCOOH + NaOH → HCOONa+h3O
то есть какую бы соду мы не добавляем к муравьиной кислоте — реакция одна и та же — кислота разлагается на воду и соль. В нашем случае соль — это формиат натрия (натриевая соль муравьиной кислоты) которая и выпадает в виде осадка.
В отличии от марганцовки, передозировка которой нежелательна, с содой проще — оставшаяся после реакции с кислотами щелочь дальше со спиртом не реагирует, и спокойно отсекается при второй перегонке. Вторая перегонка здесь необходима, поскольку соль полностью в осадок не выпадает и частично остается в растворе, и без перегонки мы получим самогон с незабываемым привкусом соды и солей органических кислот — поверьте, не самый лучший ароматизатор.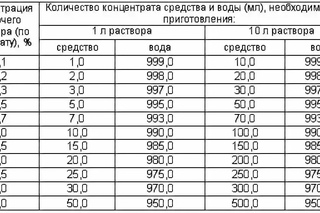
Итак, мы выяснили, что использовать можно любую соду — отличия в дозировках, давайте же выясним пропорции.
Для того, чтобы получить 1% раствор гидроксида натрия, надо в 100 г воды растворить 1 г NaOH.
Если растворить 1 г пищевой соды, то получится приблизительно 0,47% раствор NaOH.
Если растворить 1 г кальцинированной соды, получится 0,75% раствор NaOH.
Нас же в свою очередь интересуют обратные пропорции, то есть если мы используем вместо пищевой соды каустическую или кальцинированную, нужно соблюдать следующие пропорции.
Если используется каустическая сода, вместо 1 грамма NaHCO3 мы берем 0,47 гр. NaOH
Если мы используем кальцинированную, то вместо 1 грамма NaHCO3, берем 0,75 гр. Na2CO3
Экзотические варианты вроде декагидрата карбоната натрия — Na2CO3•10h3O — стиральной соды я думаю рассматривать нет смысла, потому что любой из рассмотренных выше трех вариантов дешев и легкодоступен в обычном продуктовом или промтоварном магазине.
Каустическая сода 99% гранулированная — DCS
Каустическая сода (NaOH) используется в растворах на водной основе как источник гидроксильных ионов для контроля pH. Каустическая сода является сильным основанием, которое, растворяясь в воде, диссоциирует на ионы натрия (Na+) и гидроксильную группу (ОН—).
ОСНОВНЫЕ ФИЗИЧЕСКИЕ СВОЙСТВА
| Внешний вид | Белые шарики, гранулы или кристаллы. | |
| Химическая формула | NaOH | |
| Плотность | 2130 кг/м3 | |
| pH 1% раствора | 13 | |
| 119г/100мл пресной воды (при 30°С) |
ОБЛАСТЬ И СПОСОБ ПРИМЕНЕНИ
Каустическую соду используется для поддержания или увеличения рН. Повышение рН с помощью соды каустической приводит к осаждению ионов магния (Mg2 +) и подавляет диссоциацию ионов кальция (Са2 +) в водах с повышенной жесткостью, таких как морская вода. Реагент также уменьшает коррозию и нейтрализует кислые газы, такие как диоксид углерода (СО2) и сероводород (H2S). Каустическая сода применяется в концентрации в диапазоне от 0,25 до 4 фунт / баррель (от 0,7 до 11,4 кг / м 3) с возможностью увеличения в зависимости от воды и типа бурового раствора.
Повышение рН с помощью соды каустической приводит к осаждению ионов магния (Mg2 +) и подавляет диссоциацию ионов кальция (Са2 +) в водах с повышенной жесткостью, таких как морская вода. Реагент также уменьшает коррозию и нейтрализует кислые газы, такие как диоксид углерода (СО2) и сероводород (H2S). Каустическая сода применяется в концентрации в диапазоне от 0,25 до 4 фунт / баррель (от 0,7 до 11,4 кг / м 3) с возможностью увеличения в зависимости от воды и типа бурового раствора.
В морской воде и в водах, содержащей буферные соли, возможно, потребуется более высокая концентрация каустика.
ПРЕИМУЩЕСТВА
- Экономичный и широкодоступный источник гидроксильных ионов для контроля pH.
- Эффективен при маленьких концентрациях.
- Увеличивает pH, вследствие чего уменьшается коррозия металла.
- Может быть использован в большинстве буровых растворов.
ОГРАНИЧЕНИЯ
- Малоэффективен в растворах и рассолах с высокой жесткостью (хлоркальциевые системы, некоторые типы морской воды), где из-за образования гидроксидов CA(OH)2, Mg(OH)2 происходит буферизация щелочности.

ТОКСИЧНОСТЬ И ОБРАЩЕНИЕ
Каустическая сода прошла экологическую сертификацию и допущена к применению на территории РФ в качестве компонента буровых растворов.
Следует обращаться в соответствии с требованиями MSDS и общими требованиями к транспортировке, хранению и использованию промышленных химреагентов. Рекомендуется использовать средства индивидуальной защиты (очки, перчатки) и соблюдать правила личной гигиены.
ВНИМАНИЕ! Реагент исключительно опасен при попадании на кожу и слизистые покровы, в дыхательные пути. Интенсивно реагирует с водой и кислотами. Гигроскопичен. При растворении в воде выделяет тепло. Рекомендуется добавлять Каустическую соду в раствор только с использованием специальной емкости для предварительной растворения его в пресной воде. При растворении следует добавлять NaOH в воду, а не наоборот. Запрещается ввод сухого NaОН непосредственно в раствор с использованием гидроворонок и эжекторов вручную.
УПАКОВКА И ХРАНЕНИЕ
Каустическая сода обычно поставляется в многослойных бумажных или пластиковых мешках весом 25 кг. Также может поставляться в бумажных или пластиковых барабанах или бочонках. Рекомендуется хранить в сухом прохладном месте, вдали от источников огня и воды. Открытую упаковку с Каустическая сода следует использовать немедленно ввиду высокой гигроскопичности. Высоко коррозионный материал — любые разливы или россыпи должны устраняться немедленно с использованием слабокислого раствора.
Каустическая сода — применение для чистки канализации
Каустическая сода является уникальным продуктом, позволяющим достаточно быстро и эффективно избавиться от засоров. Более известное название этого средства — щёлочь (гидроксид натрия). Её применение является одним из самых действенных инструментов для чистки канализации. Быстрорастворимая в воде щёлочь не имеет запаха и при этом легко решает проблему с засорёнными трубами.
В чём особенность каустической соды
Гидроксид натрия является активной щёлочью, имеющей вид бесцветных кристалликов. В момент соприкосновения с водой вещество начинает выделять большое количество тепла, тем самым разъедая образовавшийся на канализационных трубах налёт.
Выпускается гидроксид натрия в виде:
- порошка;
- жидкости;
- геля.
Щёлочь, смешанная с другими компонентами, используется не только как средство для прочистки канализации, но и как как моющее средство в самых разных целяхГидроксид натрия на 100% разъедает волосяной покров, отложения органического типа, которые чаще всего забивают трубы.
Применение щёлочи при чистке канализации
Каждая из трёх форм выпуска требует соблюдения определённых инструкций.
Жидкость
- Для этого способа необходимо развести каустическую соду в воде в соотношении 2 кг соды на 4 л воды (для частного дома — 3 кг на 7 л).
- Половину подготовленного раствора влейте в слив (постарайтесь сделать это максимально аккуратно и не попадите на эмаль).
- Не пользуйтесь сливом примерно 3 часа.
- Затем также осторожно влейте оставшуюся половину жидкости и промойте слив сильным напором проточной холодной (!) воды. Промывать слив нужно около 15 минут.
Для профилактики более чем достаточно применять компонент 1–2 раза в месяц.
Порошок
Принцип использования порошка схож с предыдущим способом. Разница лишь в том, что при данном методе все реакции будут протекать непосредственно в трубах.
- Включите горячую воду и оставьте её минут на 15–20, чтобы слегка прогреть трубы.
- Насыпьте в сливное отверстие половину стакана содового порошка.
- Откройте холодную воду и оставьте её на 35–45 секунд.
- После всех манипуляций закройте кран и не пользуйтесь сливом в течение 2–3 часов.
- Включите холодный кран и оставьте его открытым на 20 минут, чтобы смыть налёт.
Гель
Для удобства покупателей выпускается готовое средство для очистки труб в форме геля. Его не нужно заранее разводить или как-то подготавливать.
- Влейте немного геля в слив, как предусмотрено в инструкции (стандартно требуется примерно 250–350 мл геля). Оставьте средство на 2–3 часа. В это время нельзя пользоваться сливом.
- После всех манипуляций промойте сильным напором холодной воды сливное отверстие в течение 15–20 минут.
Меры предосторожности
Поскольку щёлочь является едким веществом, применять её нужно с большой осторожностью, соблюдая при этом определённые правила:
- обязательно надевайте плотную маску, резиновые перчатки и очки, чтобы избежать попадания средства на кожу или слизистые;
- соблюдайте инструкции и пропорции во время работы с веществом.
Если по какой-то причине сода попадёт на кожный покров или слизистые, то могут возникнуть серьёзные ожоги (при попадании в глаза возможна полная потеря зрения). В таком случае нужно тщательно промыть слизистые оболочки слегка тёплой проточной водой и обратиться к врачу.
Видео: прочистка канализации едким натром
Щёлочь является одним из самых эффективных и простых в применении средств для борьбы с засорами. Главное при её использовании соблюдать пропорции и меры предосторожности.
Оцените статью: Поделитесь с друзьями! Смотрите также:Как развести каустическую соду для промывки радиатора
Каустическая сода или гидроксид натрия представляет собой химическое вещество, которое имеет в народе множество названий. Продается оно в виде белого порошка, геля или гранул.
Помимо этого существуют специальные средства, в составе которого содержится это вещество. Каустик обладает хорошими разъедающими свойствами. Именно поэтому его широко используют для промывки различных систем. Но, чтобы добиться максимального эффекта, необходимо разобраться, как именно проводятся промывочные работы.
Промывка котлов
В процессе производства, установки и эксплуатации котла внутри него могут образоваться вещества, которые в результате негативно скажутся на работе всей системы. Устранить такие примеси можно с помощью каустической соды.
Помимо этого ее применяют после обработке агрегата кислотами. Каустик снижает риск возникновения налета и накипи.
Промывка котла проводится по довольно простой схеме:
- заполнить агрегат водой;
- добавить соду;
- нагреть котел до определенной температуры и поддерживать его в таком состоянии до 24 часов;
- слить воду и провести окончательную чистку оборудования.
При проведении очистительных работ стоит тщательно рассчитать, сколько активного вещества понадобится для этого. Так, на 1 м3 воды пойдет близко 9 кг каустической соды. При выполнении чистки стоит следовать основным правилам безопасности.
Очистка радиаторов
Жители многоэтажных домов старой постройки часто сталкиваются с такой проблемой, как плохое отопление жилого пространства.
Часто такие проблемы возникают на фоне загрязнения радиаторов отопительной системы. Из-за этого они не способны пропускать достаточное количество теплоносителя и тем сам нагреваться до нужной температуры.
Промывка радиаторов осуществляется несколькими способами. Если нет возможности провести работу специальными аппаратами, то для этого используют щелочи. Прежде всего, нужно демонтировать батарею. Лучше всего работы проводить в ванной.
Процесс осуществляется в такой последовательности:
- С помощью шланга или лейки внутрь заливается горячая вода. Заглушки нужно открыть, чтобы грязная вода беспрепятственно выходила из батареи. Когда воды в ней будет достаточно, необходимо хорошенько встряхнуть. Обработка проводится до тех пор, пока большие куски не будут извлечены.
- Залить каустик. Когда реакция закончиться, батарею снова встряхнуть. Для этого можно слегка постукать по ней резиновым или деревянным молотком. Это значительно улучшит качество очистки.
- Вымыть радиатор проточной водой. Это нужно делать до тех пор, пока не исчезнет пена или запах щелочи.
По окончанию проводится монтаж отопительного элемента на место, после чего нужно проверить его в действии.
Промывка системы отопления
В процессе эксплуатации отопительной системы возможно ее засорение известковыми, окисными и илистыми отложениями. В результате этого температурные показатели снижаются. Возможно и полный ее выход из эксплуатации. Если своевременно не выполнить очистительные работы, то это может привести к катастрофическим последствиям.
Обладая определенными навыками и знаниями, с такой работой сможет справиться каждый самостоятельно.
Сам же процесс чистки выглядит примерно так:
- Контур промывают водопроводной водой, после чего вводят в нее каустическую соду. Щелочная среда легко удаляет с внутренних поверхностей накипь и коррозию.
- На следующем этапе выполняется промывка технической водой. Далее проводится введение в отопительный контур химического реагента. Он прогоняется по кругу несколько раз. При этом нужно проследить за тем, чтобы температура поддерживалась на нужном уровне. Таким образом, удаляются многослойные отложения, которые препятствуют нормальному прохождению теплоносителя.
- Далее система второй раз промывается технической водой. После этого повторно вводится щелочь для того, чтобы нейтрализовать остатки кислотных примесей. Такая последовательность обработки позволяет в дальнейшем предотвратить коррозийные процессы внутри системы.
- На завершающем этапе проводится промывка сначала технической, а затем водой из центральной системы водоснабжения. В заключение из контура сливается вся жидкость. При этом нужно удостовериться в том, что в нем не осталось остатков чистящего вещества.
Важность промывки системы охлаждения двигателя очевидна. Если кто-то из водителей этого еще не понимает, то сразу пересаживайтесь на гужевой транспорт, он точно не перегреется и не подведет.
Из статьи вы узнаете как промыть систему охлаждения водой, лимонной кислотой, уксусом, каустической содой, молочной кислотой, сывороткой, кока-колой, специальной автохимией, поговорим про ошибки, который не следует допускать.
Последствия неправильного ухода за системой охлаждения
Система охлаждения (СО), это важный элемент любого автомобиля, особенно если охлаждение его двигателя жидкостное.
Неправильное ее функционирование может привести к непоправимым последствиям, а это:
- Перегрев двигателя, и как следствие, полный выход его из строя;
- Поломка подогревателя тосола или другого аналогичного устройства;
- Выход из строя помпы;
- Малоэффективная работа печки салона.
Как правило, причина в неэффективной работе жидкостной системы охлаждения любого автомобиля лежит в загрязнении радиатора, патрубков, полостей рубашки охлаждения блока цилиндров.
Если бы мы смогли проникнуть вовнутрь данной системы, то увидели интересную картину.
Ржавчина, отложения накипи на стенках, остатки от разложенной охлаждающей жидкости, жирные пятна от масла и другие неприятности.
Стоит отметить, что речь идет об двигателях бывших в эксплуатации от 2 – х лет и более. Про новые автомобили здесь речь не идет.
Когда нужно промывать систему охлаждения двигателя?
Промывать систему охлаждения двигателя рекомендовано один раз в два–три года, в зависимости от интенсивности эксплуатации автомобиля.
Нужно понимать, что любая охлаждающая жидкость (ОЖ), будь то тосол или антифриз, со временем теряет свои эксплуатационные качества.
Происходит разложение жидкости на отдельные химические элементы, одни из которых выпадают в осадок и частично перекрывают каналы, по которым она же и циркулирует, другие оседают на стенках в виде накипи.
Как следствие, антифриз или тосол через один-два года эксплуатации, за единицу времени начинают меньше забирать тепло от двигателя.
Период обращения жидкости по кругу увеличивается и КПД работы всей системы уменьшается.
Поэтому, чтобы у вас в дороге не возникали проблемы с перегревом двигателя, при каждой новой замене охлаждающей жидкости следует делать промывку всей системы.
Какой способ промывки выбрать
Нужно понимать, что способов промывки системы охлаждения двигателя несколько:
- Дистиллированной, кипяченной или подкисленной водой;
- Промывка специальными средствами.
В зависимости от степени загрязнения применяются различные способы промывки.
Определяем степень загрязнения.
Слейте тосол или антифриз и оцените его состояние. Если в жидкостях будут наблюдаться частицы ржавчины, окиси, жирные пятна, цвет будет темный или черный, то степень загрязнения большая.
В данной случае для получения максимального результата придется применять подкисленную воду или специальные средства.
Если отработанная охлаждающая жидкость имеет больше светлого оттенка, чем темного, без явного наблюдения осадков, то смело можно использовать дисцелированную или кипяченую воду.
Промывка системы охлаждения водой
Оденьте резиновые перчатки, чтобы кожа рук не соприкасалась с вредной жидкостью. Поднимите капот и откройте расширительный бачок.
Слейте старую охлаждающую жидкость из системы. Для этого выкрутите пробку (болт) на блоке цилиндров и откройте краник на радиаторе.
Верните пробку (болт) и краник в исходной положение. Сильно не зажимайте их.
Залейте через расширительный бачок дистиллированную или кипяченую воду согласно норме.
Заведите двигатель. 15 – 20 минут его работы на пониженных оборотах будет достаточным.
Слейте воду обратив внимание на ее состояние. Если вода грязная, значит повторите процедуру. Добейтесь, чтобы сливаемая вода была чистой.
Только потом заливайте свежие антифриз или тосол.
Использование подкисленной воды
Если в старой охлаждающей жидкости наблюдаются частицы накипи, ржавчины и т.д., то можно сделать вывод, что обычная вода с очисткой системы охлаждения не справиться.
Нужно использовать более агрессивные средства и тут подойдет подкислённая вода.
В качестве окислителя можно использовать столовый уксус, лимонную кислоту, каустическую соду или молочную кислоту.
Дело в том, что лимонная кислота вступает в реакцию только при больших температурах, 70 – 90 градусов.
Также очень важно правильно подготовить раствор, чтобы не навредить резинотехническим изделиям и металлу.
Обычно в 5 литров воды засыпают 100 – 120 грамм лимонной кислоты, соответственно на 4 литра – 80 — 100 грамм. Если не хотите рисковать, пропорцию можно уменьшить.
Другие водителя наоборот увеличивают пропорцию. Но указанные цифры наиболее оптимальные.
Алгоритм действий тот же. Сливаем старую ОЖ и заливаем подготовленный раствор. Далее, заведите двигатель прогрейте его. Проедьтесь на автомобиле пару километров.
Это делается для того, чтобы температура раствора поднялась до нужной нам в 70 – 90 градусов и произошла необходимая реакция. Работать двигатель должен 30 – 40 минут.
Далее сливаем, отработанный раствор и анализируем результат. При необходимости повторите промывку, но уже с более слабым раствором.
На окончательном этапе промойте систему охлаждения дистиллированной или кипяченой водой, чтобы удалить остатки лимонной кислоты.
Если вы решили использовать столовый уксус, то тут тоже нужно знать правильную пропорцию раствора.
К примеру, в 10 литров воды вливается 500 мл столового уксуса. Полученный раствор заливают в систему охлаждения. Заводят автомобиль и прогревают двигатель до рабочих температур.
После этого выключаем зажигание и оставляем прогретый раствор в двигателе на ночь или 8 часов.
Сливаем, смотрим результат. При необходимости повторяем. В конце обязательно промываем дистиллированной водой.
При очень тяжелых случаях, некоторые водителя сразу заливают 9% столовый уксус, не разбавляя. Для нескольких раз придется купить 20 бутылок по 0,5 литра.
Если используете уксусную кислоту, то она имеет 70% концентрации, учтите это.
Каустическая сода применяется только для промывки снятых медных радиаторов системы охлаждения двигателя и радиаторов печки салона.
Если у вас данные устройства алюминиевые, что свойственно для многих современных автомобилей, то забудьте про этот вариант.
Двигатель каустической содой не промывается, так как, многие знают, что головка блока цилиндров изготовлена из алюминия, да и прокладки под головкой будут разъедены.
Если ваш радиатор не подпадает под категорию алюминиевый, то для его промывки можно использовать раствор каустической соды из расчета на 1 литр дистиллированной воды, 50 – 60 гр. вещества. Но перед промывкой его желательно снять.
Такой способ дает неплохой результат, но тут тоже нужно уметь правильно подготовить раствор.
Но проблема даже стоит не в этом, а в том, где достать молочную кислоту, ведь в свободной продаже ее трудно найти.
Если в вашем городе есть возможность ее достать, то отлично.
Также на специализированных автофорумах, особенно по бу автомобилям, можно найти людей, которые продают молочную кислоту. В общем, как говориться, было бы желание.
Для прочистки системы охлаждения нужен 6% раствор молочной кислоты. Как правило, концентрат имеет 36%.
Но расчет тут прост, делаем соотношение 1:5, т.е. в 5 литров дистиллированной воды заливаем 1 кг концентрата, получив этим нужные проценты.
Дальше можно пойти двумя путями:
- Залить раствор молочной кислоты и дождаться пока прекратиться выделение углекислого газа, затем слить отработанную смесь;
- Проехать на автомобиле несколько километров, затем слить грязную смесь.
Многие водителя ездят с залитой молочной кислотой сутки, сливают, заливают снова и опять ездят.
Так тоже можно делать, ведь молочная кислота не так агрессивно воздействует на алюминий и резинотехнические изделия.
Однако при этом было замечено, что двигатель начинает сильно греться, больше обычного.
Это происходит потому, что, выделяясь, углекислый газ создает в патрубках и блоке цилиндров, так называемые воздушные пробки.
Поэтому нужно быть осторожным и более внимательно следить за показаниями панели приборов.
В конце не забудьте нейтрализовать кислотность. Для этого лучше использовать 0,5% раствор хромпика или дистиллированную воду. Двигатель должен поработать 10-20 минут.
Только после этого заливайте новую охлаждающую жидкость.
Неплохая альтернатива молочной кислоте. Сначала сыворотку процеживают, в емкость не менее 5 л.
Затем заливают через расширительный бачок в систему охлаждения.
Ездят с сывороткой 1000-1500 км, затем ее сливают. При необходимости цикл повторяют. Однако каждые 100-200 км пробега рекомендуется проверять степень загрязненности сыворотки.
Постоянно нужно следить за температурой двигателя.
Как это ни странно звучало, но раньше промывка системы охлаждения кока-колой давала неплохой результат.
Эффект достигался за счет входящей в состав напитка ортофосфорной кислоты.
Но по слухам, сейчас эту кислоту в Соса-соlа не добавляют, поэтому прошлого эффекта ожидать уже не приходиться.
Но перепроверку слухов никто не отменял, вреда двигателю Соса-сола точно не нанесет.
Используемые средства – авто химия
Преимущество средств для промывки системы охлаждения в том, что они идут в ногу со временем.
Их состав разрабатывается таким образом, чтобы не навредить двигателю. К примеру, для медных радиаторов раньше использовали одни средства, сейчас для алюминиевых, другие. Или комбинированные для всех типов двигателей.
Стоят они недорого, поэтому практически каждый владелец автомобиля может себе позволить купить такое средство.
Неплохо удаляет самые сложные загрязнения системы охлаждения. Флакона в 250 мл хватит на три раза промыть СО малолитражки или два раза автомобиля с большим объемом двигателя.
Характеристики Radiator Flush.
LAVR Radiator Flush 1&2.
Еще одно неплохое средство для прочистки системы охлаждения. Пользуется популярностью за хорошее соотношение цена и качество.
Это промывочный комплекс, в который входит два состава.
Первый состав. Борется со ржавчинной и накипью. Хорошо убирает их и выводит из системы.
Второй состав. Ликвидирует масляные отложения и растворяет жиры.
Комплекс нейтрален к резинотехническим изделиям, пластику и всем видам металлов.
Применение LAVR Radiator Flush 1&2.
Не забудьте, на завершающем этапе, промойте СО дистиллированной или кипяченой водой.
Существую много и других аналогичных промывочных средств, но прежде, чем их использовать читайте отзывы на формах.
Основные ошибки при промывке СО двигателя
- Работы проводятся в холодную погоду, когда ночью возможны заморозки;
- Не одеваются перчатки в итоге можно получить тепловой или химический ожог;
- Неправильный анализ отработанной ОЖ, что приводит к перерасходу средств на промывку или к неверному подбору средств. К примеру, каустическая сода для промывки алюминиевых радиаторов не применяется;
- Неправильно подобранная концентрация промывочного раствора, что может привести к разъеданию резинотехнических изделий и появлению дополнительной ржавчины;
- Забывчивость. На завершающим этапе не забывайте промывать систему охлаждения нейтральными жидкостями, к примеру, водой – дистиллированной или кипяченной;
- Заливайте только качественную ОЖ, исключите подделки. Читайте тут, как выбрать антифриз.
Подводим итог
Промыть систему охлаждения двигателя несложно, главное это делать с определенной периодичностью.
Также нужно грамотно использовать промывочные средства, включая и правильное составление растворов.
Покупную авто химию использовать проще, главное, действовать согласно инструкции и результат будет не хуже. Что мы и рекомендуем делать.
Свои идеи и замечания оставляйте в комментариях.
Собсно после удачной пробной попытки чистки радиатора печки каустической содой — дошли руки )) до радиатора охлаждения. По тексту буду немного повторяться, для читабельности.
Почему каустической содой? Потому, что так пишет книга по ремонту! Захотелось попробовать.
И так, мы имеем сам радиатор, который перед манипуляцией чистки каустиком — нужно как следует промыть проточной водой (желательно под хорошим давлением) сначала против направления движения ОЖ потом за ним, так хорошо удаляются слоистые отложения у которых «зацеп» водой происходит лучше когда вода идет против движения ОЖ в системе.
На это у меня ушло около часа, при чем уже после 20-ти минут промывки вода была уже чистой, но на протяжении оставшихся 30-40мин из радиатора продолжали вылетать твердые частицы отложений.
Для этого использовал весы, стекляную банку (3-х литровую) и воду )) В радиатор охлаждения влазит 4,5л
После этого влил в него все 4,5л укропа )) и поставил таймер на 40мин. Результат не заставил себя долго ждать — начало все бурлить в радиаторе, плеваться пеной стал, а я тем временем как ребенок бегал возле него и радовался ))
Через 40мин я вытянул палку и наблюдал как с радиатора повалила жижа цвета каштана ))) А еще понял что тупонул и не заснял сие чудо )) Но вы можете лицезреть )) какого цвета стала палочка-выручалочка.
Далее снова проточной водой под давлением около 30мин все вымывал до появления кристально чистой воды.
Вот собственно и весь процесс, он не затратный и в то же время очень прост!
Снова напоминаю — Все выше описанное относится только к снятым МЕДНЫМ радиаторам, т.к. каустическая сода разъедает алюминий! Не заливайте в систему охлаждения!
p.s. Сначала решил не заморачиваться но после чистки, все же отвез на перепайку верхнего бачка, т.к. спаян был с применением колхоза и бачок был деформирован, что мне не нравилось! За одно проверили герметичность радиатора перед пайкой — все ГУД! )) нигде не травило.
После вскрытия пайщик подтвердил что радиатор абсолютно чистый, шомполом все же прошелся по каналам — каки не обнаружил! Фото нету, я отсутствовал в это время.
ЖМЕМ ЗАВЕТНУЮ КНОПОЧКУ — нравится! )) А если еще и поделитесь со всеми — точно не напрасно труды мои прошли!
ВСЕМ СПАСИБО!
Как приготовить раствор гидроксида натрия или NaOH
Гидроксид натрия — распространенное и полезное сильное основание. Требуется особая осторожность при приготовлении раствора гидроксида натрия или NaOH в воде, поскольку в результате экзотермической реакции выделяется значительное количество тепла. Раствор может разбрызгиваться или закипать. Вот как безопасно приготовить раствор гидроксида натрия, а также рецепты для нескольких распространенных концентраций раствора NaOH.
Количество NaOH для приготовления раствора гидроксида натрия
Приготовьте растворы гидроксида натрия, используя эту удобную справочную таблицу, в которой указано количество растворенного вещества (твердый NaOH), которое используется для приготовления 1 л основного раствора.Следуйте этим правилам безопасности в лаборатории:
- Не трогайте гидроксид натрия! Он едкий и может вызвать химические ожоги. Если на кожу попал NaOH, немедленно промойте его большим количеством воды. Другой вариант — нейтрализовать любую основу на коже слабой кислотой, например уксусом, а затем смыть водой.
- Размешайте гидроксид натрия понемногу в большом объеме воды, а затем разбавьте раствор до одного литра. Добавьте гидроксид натрия в воду — не добавляйте воду к твердому гидроксиду натрия .
- Обязательно используйте боросиликатное стекло (например, Pyrex) и подумайте о том, чтобы погрузить контейнер в ведро со льдом, чтобы снизить температуру. Осмотрите стеклянную посуду перед использованием, чтобы убедиться, что на ней нет трещин, царапин или сколов, которые могут указывать на слабость стекла. Если вы используете стекло другого типа или непрочное стекло, есть вероятность, что изменение температуры может привести к его разрушению.
- Надевайте защитные очки и перчатки, так как существует вероятность разбрызгивания раствора гидроксида натрия или разрушения стеклянной посуды.Концентрированный раствор гидроксида натрия вызывает коррозию и требует осторожного обращения.
Дополнительная ссылка
- Курт, Цетин; Биттнер, Юрген (2006). «Гидроксид натрия.» Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. DOI: 10.1002 / 14356007.a24_345.pub2
Рецепты обычных растворов NaOH
Чтобы приготовить эти рецепты, начните с 1 литра воды и медленно добавьте твердый NaOH.Магнитная мешалка будет полезна, если она у вас есть.
| М раствора | Количество NaOH | |
|---|---|---|
| Гидроксид натрия | 6 месяцев | 240 г |
| NaOH | 3 Месяца | 120 г |
| F.W. 40,00 | 1 Месяц | 40 г |
| 0,5 млн | 20 г | |
| 0.1 М | 4,0 г |
Безопасное разбавление гидроксида натрия | TACMINA CORPORATION
Заказчик
Производитель химикатов
Потребности и проблемы клиента
Мы хотим безопасно разбавить гидроксид натрия с концентрации 48% до концентрации 25%.
- Во время разбавления выделяется значительное количество тепла, что создает риск разбрызгивания жидкости.
- Жидкость опасна, так как при контакте с человеческим телом может привести к серьезным увечьям.
Решения TACMINA
Была создана система, в которой жидкость перекачивается с помощью насоса Smoothflow, а статический смеситель используется для поточного смешивания.
- Жидкость не контактирует с воздухом, что обеспечивает безопасное разбавление.
- Непрерывный постоянный поток без пульсаций стабилизировал концентрацию разбавленного раствора.
- Тепло разбавления можно отводить с помощью теплообменника для охлаждения.
- Устранена необходимость в баке для разбавления, что позволило использовать систему в меньшем пространстве.
Блок-схема
Товар
- БПЛ
- Макс. объем разгрузки
- 0,05 ~ 80 л / мин
- Макс. давление нагнетания
- 1.0 МПа
Идеально подходит для перекачки различных химикатов и жидкостей на большие расстояния / с большим напором, например химикатами для очистки воды и полимерными коагулянтами
- Тип с прямым приводом
- Высокая емкость
- Разбавитель серной кислоты
К началу страницы
Каустическая сода — Любопытный гравер
Легко нервничать, когда вы читаете некоторую информацию о каустической соде.Это потенциально опасно, как и ремесленный нож, поэтому важно понимать его свойства и безопасно использовать его.
Что такое каустическая сода?Бутылка каустической соды
Каустическая сода представляет собой крупный белый порошок, который образует сильную щелочь, когда вы добавляете его в воду.
Химическое вещество — гидроксид натрия, NaOH.
Чаще всего он используется в домашних условиях для разблокировки сточных вод, хотя существует также множество промышленных и пищевых применений.
Каустическая сода разлагает белки. Белки — это живые (или живые) объекты, например ткани растений и животных, например, натуральные масла и жиры, волосы и кожа. Это также относится к вам!
Попадание на кожу вызывает болезненные химические ожоги.
Он не влияет на искусственные материалы (но может повлиять на алюминий), поэтому для его смешивания используйте пластиковые контейнеры, резиновые перчатки и пластиковые фартуки, скатерти и т. Д.
Где взять?
Ваш местный хозяйственный магазин или магазин поделок предоставит его в качестве очистителя канализации. Храните его в оригинальном контейнере и четко маркируйте всю смешанную каустическую соду.
Приготовление каустической соды
защитное снаряжение из синтетических материалов
Вы можете смешивать щелочные растворы разной силы в зависимости от того, для чего вы их используете.
Налейте воду в пластиковый контейнер и всегда добавляйте порошок к воде , а не наоборот.(Существует опасность «взрыва» смеси и разбрызгивания).
Происходит химическая реакция; он становится горячим и выделяет пары примерно через 30 секунд после смешивания — на этом этапе будьте очень осторожны.
Используйте резиновые перчатки, закрывающие запястья, и наденьте очки в хорошо вентилируемом месте при смешивании.
При попадании на кожу смойте большим количеством воды в течение 10–15 минут.
Прочтите инструкции по технике безопасности на контейнере перед использованием каустической соды.
Если все это звучит довольно опасно, не бойтесь — просто будьте благоразумны и убедитесь, что вы хорошо подготовлены.
Немного истории….
Средневековое мыло из щелока
С раннего средневековья гидроксид натрия получали путем сжигания богатых натрием растений с последующим процеживанием воды через пепел. Жидкость, известная как щелок или кальцинированная сода, используется с натуральными маслами или гусиным жиром для изготовления мыла.
Вы можете попробовать это, если хотите быть по-настоящему самодостаточным.….
Как печатники используют это?Есть несколько способов использования каустической соды в гравюре;
- Линно-травление
Традиционный линолеум изготавливается из льняного масла и мела. Льняное масло является натуральным белком, поэтому его растворяет каустическая сода.
Если вы попробуете его на виниловом линоле «soft cut», то никакого эффекта не будет, так как оно синтетическое и не содержит белков. Посмотрите, как это сделать, на посте «Лино-травление».
- Производство бумаги
Чтобы сделать бумагу из растений, нужно отделить мягкие ткани от более прочных волокон, каустическая сода сделает это за вас.
Будьте смелыми!
Каустическая сода — это сильнодействующее химическое вещество, которое отлично подходит для травления линз. Как и многие другие полезные вещества, он также несет в себе опасность, но если вы спланируете свое рабочее пространство, поймете риски и будете использовать его осторожно, вы сможете создавать красивые текстурированные линолеумные пластины.
ГИДРОКСИД НАТРИЯ — Пределы аварийного и непрерывного воздействия для отдельных загрязняющих веществ, переносимых по воздуху
Токсичность гидроксида натрия зависит от концентрации раствора гидроксида натрия и продолжительности его контакта с тканями. Химическое вещество действует локально, оказывая сильное разъедающее действие, механизм которого неизвестен, и вызывает почти немедленную дегенерацию тканей, что может привести к быстрому всасыванию гидроксида натрия в систему кровообращения и распределению с водой тела.Он полностью диссоциирует в воде, крови и цитоплазме и не метаболизируется.
Поскольку токсичность гидроксида натрия определяется в первую очередь концентрацией гидроксильного иона, общая щелочность снижается, когда образуется карбонат натрия (Na 2 CO 3 ). Следовательно, измерение концентрации ионов натрия не всегда является точным показателем щелочности и токсического потенциала (Cooper et и ., 1979).
ВЛИЯНИЕ НА ЧЕЛОВЕКА
Люди могут подвергаться воздействию при производстве гидроксида натрия и при обращении с гидроксидом натрия в виде твердого или концентрированного раствора.
Гидроксид натрия оказывает разъедающее действие на все ткани организма; концентрированные пары вызывают серьезное повреждение глаз и дыхательной системы. Проглатывание гидроксида натрия, которое часто встречается у детей, может вызвать тяжелый некроз со стриктурой пищевода и смертью. Контакт с кожей может привести к дерматиту, выпадению волос и некрозу из-за раздражения. Типы кожи различаются по чувствительности к едкому раздражению.
Переносимые по воздуху туманы гидроксида натрия вокруг чанов для обезжиривания (при 200 ° F), содержащих Seco 75 или Tysol 810 (концентрированные растворы гидроксида натрия в сочетании с хелатирующими и смачивающими агентами), были связаны с раздражением верхних дыхательных путей у рабочих, подвергшихся воздействию гидроксида натрия при температуре 0.01-0,7 мг / м 3 (среднее 0,1-0,15 мг / м 3 ). Рабочая зона также содержала пары растворителя Стоддарда, масла ENSIS 254, Zyglo и растворов Magna-flux (концентрации растворителя Стоддарда в воздухе составляли 13-780 мг / м 3 ) и, во время очистки ванны, серной кислоты с концентрацией 0,1- 0,6 мг / м 3 (Hervin and Cohen, 1974). Влияние этих хелатирующих агентов и растворителей на токсичность гидроксида натрия неизвестно.
Отт и и . (1977) оценили уровень смертности среди сотрудников химических заводов, хронически подвергающихся воздействию едкой пыли.Записи об остром воздействии (неизвестные концентрации) показали, что едкие вещества в растении вызвали реакцию от легкой до тяжелой (раздражение, эритема и «объективное повреждение органов») кожи, глаз и дыхательной системы. Никаких указаний на чистоту дано не было, но было отмечено, что хлорид натрия и карбонат натрия, как известно, были включены в воздействие щелочи; рабочие, которые, как известно, подвергались воздействию мышьяка или асбеста, а также щелочи, были исключены из исследования. Согласно результатам исследования, в ходе которого измерялась общая щелочность проб воздуха на рабочем месте, концентрация гидроксида натрия достигает 6.7 мг / м 3 на одном участке растения хорошо коррелировали с данными субъективного ответа, которые указывали на усиление раздражения дыхательных путей с увеличением концентрации щелочи; на втором участке завода, где содержание гидроксида натрия составляло до 7,7 мг / м 3, корреляция была плохой. Никакого объяснения плохой корреляции найти не удалось. Гидроксид натрия с концентрацией до 2 мг / м 2 3 (TWA) действительно вызывает раздражение носа и кожи, особенно на участках растений с высокими температурами.Поправочный коэффициент для влияния температуры на токсичность гидроксида натрия отсутствует, но ожидается, что повышение температуры приведет к увеличению токсичности.
Контролируемое воздействие растворов гидроксида натрия ограничивалось кожным нанесением, обычно на предплечья добровольцев. Мальтен и Спруит (1966) поместили 0,12% (0,03 М) или 0,27% (0,0675 М) растворы гидроксида натрия в чашки, прикрепленные к предплечьям добровольцев. Эритема вызывалась в течение 0,5 часа более сильным раствором и в течение 1 часа более разбавленным препаратом (см. Также Spruit and Malten, 1968).Марзулли и Майбах (1975) наносили растворы гидроксида натрия на спину людей в закрытых пластырях, обновляемых ежедневно в течение 21 дня. Самая низкая изученная концентрация (0,05%, 0,0125 М) не вызывала эритемы, 0,5% (0,125 М) раствор оказывал умеренное раздражение, а растворы 4% или 5% вызывали сильное раздражение. Аналогичные результаты наблюдались у кроликов.
Приготовление стандартного раствора гидроксида натрия *
Д-р Мурли Дхармадхикари и Тавис Харрис
Примечание. Эта статья написана по запросу представителей отрасли.Он написан для сотрудников винных лабораторий без химического образования.
В винной лаборатории анализ вина на TA, VA и SO2 включает использование реактива гидроксида натрия (NaOH). Виноделы обычно покупают раствор гидроксида натрия известной концентрации (обычно 0,1 нормального). Этот реагент относительно нестабилен, и его концентрация со временем меняется. Для обеспечения точности аналитических результатов важно периодически проверять концентрацию (нормальность) гидроксида натрия.Если концентрация изменилась, ее необходимо отрегулировать до исходной концентрации или в расчетах необходимо использовать новое значение концентрации (нормальность).
Иногда винодел может захотеть сделать свой собственный раствор NaOH вместо того, чтобы покупать его. При приготовлении нового раствора или проверке нормальности старого раствора важно знать процедуру приготовления стандартного (известной концентрации) раствора реагента NaOH. В данной статье объясняется процедура стандартизации, а также основная концепция процедуры титрования.
Выражение концентрации в растворе
Раствор состоит из растворенного вещества и растворителя. Растворенное вещество — это растворенное вещество, а растворитель — это вещество, в котором растворенное вещество растворено. Растворенное вещество может быть твердым или жидким. В растворе NaOH гидроксид натрия (твердый) является растворенным веществом, а вода (жидкость) является растворителем. Обратите внимание, что растворенное вещество, являющееся твердым веществом, измеряется в единицах веса (в граммах), а вода-растворитель измеряется в единицах объема. Это пример выражения веса раствора на единицу объема (вес / объем).
В растворе, состоящем из двух жидкостей, концентрация выражается в объемах на объемную основу. Например, концентрация алкоголя в вине выражается как объем на объем. Вино с 12% -ным содержанием алкоголя означает, что оно содержит 12 мл алкоголя на 100 мл вина.
Обычно во многих растворах вес указывается в граммах, а объем — в миллилитрах или литрах. На этом этапе важно установить соотношение между единицами веса и объема. Один килограмм (вес) воды при температуре максимальной плотности и нормальном атмосферном давлении имеет объем один литр.Это означает, что один килограмм (вес) воды равен одному литру объема, а один грамм воды по весу равен одному миллилитру воды по объему. Таким образом, единицы веса (грамм) и объема (мл) похожи и взаимозаменяемы.
Химик выражает концентрацию раствора по-разному. Общие выражения включают в себя процент, частей на миллион (ppm), молярный и нормальный. Важно четко понимать эти термины.
Процент
Одна из простейших форм концентрации — это процент.Это просто означает единицы на 100 единиц или частей на 100 частей. Процентную концентрацию можно использовать тремя способами. Это может быть масса на единицу веса, объем на объем или масса на единицу объема.
Когда виноделы используют ареометр ° Brix для измерения сахара в виноградном соке, они, по сути, измеряют граммы сахара на 100 граммов сока. Образец сока 18 ° Брикса означает 18 граммов сахара на 100 граммов сока или обычно обозначается как 18%. При описании содержания алкоголя в вине процентное содержание алкоголя выражается в единицах объема на объем.Во многих случаях, в том числе в лаборатории, раствор получают путем растворения твердого вещества в жидкости, обычно в воде. В таком случае концентрация выражается в расчете на объемный вес.
Частей на миллион
Когда мы имеем дело с очень небольшим количеством вещества в растворе, концентрация часто выражается в частях на миллион. Концентрация 20 ppm означает растворение 20 частей растворенного вещества на каждые 1000000 частей раствора. Единицей измерения может быть вес или объем.Обычно концентрация ppm используется для обозначения миллиграммов растворенного вещества на литр раствора.
Молярный раствор
Молярный раствор означает концентрацию в моль / литр. Один молярный (I M) раствор означает один моль вещества (растворенного вещества) на литр раствора. Моль означает молекулярную массу в граммах или молекулярную массу вещества в граммах. Таким образом, молекулярная масса химического вещества также является его молярной массой. Чтобы рассчитать молекулярную массу, нужно сложить атомные массы всех атомов в молекулярной формульной единице.Например, молекула NaOH состоит из одного атома натрия (Na), кислорода (0) и водорода (H). Их соответствующие атомные массы: Na — 23,0 — 16 и H — 1, поэтому молекулярная масса составляет 23 + 16 + I = 40. Таким образом, 40 граммов NaOH равны одному моль NaOH, а 1 молярный раствор NaOH. будет содержать 40 граммов химиката NaOH.
Нормальный раствор / Нормальность
Другой формой концентрации, которая используется относительно часто, является нормальность, или N. Нормальность выражается в эквивалентах на литр, что означает количество эквивалентных весов растворенного вещества на литр раствора.Термин нормальность часто используется в кислотно-щелочной химии. Эквивалентная масса кислоты определяется как молекулярная масса, деленная на количество реагирующих атомов водорода одной молекулы кислоты в реакции.
Чтобы понять эквиваленты, нужно знать кое-что о том, как работает реакция, так что давайте начнем с этого. Ниже приведено основное уравнение для кислоты и основания.
HCl + NaOH ——> NaCl + h30
или
Кислота + основание ——-> соль + вода
В нашем простом уравнении, приведенном выше, вы можете видеть, что кислота и основание реагируют с образованием соли и воды, и что они реагируют одинаково.Кислота дает 1 H + на каждый -OH, заданный основанием. Таким образом, на каждый моль H + нужно
моль.-ОН. Эта реакция является взаимно однозначной на молярной основе. Один моль кислоты имеет одну реакционную единицу, а один моль основания также имеет одну реакционную единицу, таким образом, как кислота, так и основание, в приведенном выше примере, имеют равные реакционные единицы 1: 1. Как указано выше, для кислот мы определяем эквивалентную массу как молекулярную массу, деленную на количество H +, выделенного на молекулу. Выше HCl отдавал в реакцию 1 H + (протон).
Молекулярная масса h3SO4 = 98,08 г = 49,04 грамма на эквивалент
Количество протонов на 2 протона
Нормальность — это молекулярная масса, деленная на граммы на эквивалент (все это приводит к количеству эквивалентов) в данном объеме. Для 1 н раствора нам нужен 1 эквивалент / литр. Для соляной кислоты (HCl) эквивалентный вес составляет 36,46 грамма. Следовательно, для приготовления 1 нормального раствора необходимо 36,46 г / л HCl. Обратите внимание, что 1 M решение также равно 36.46 г / л. Для молекул, которые могут выделять или принимать только один протон на молекулу, нормальность равна молярности.
Таблица 1. Молекулярная и эквивалентная масса некоторых распространенных соединений.
В случае, если молекула может испускать или принимать более одного протона, вам необходимо скорректировать свои вычисления. Например, серная кислота с формулой h3SO4 отдает 2 отдельных протона. Используя молярную массу серной кислоты и зная, что одна молекула может отдавать 2 протона, мы можем найти эквивалентную массу.
При молярной массе 98,08 грамма раствор, содержащий 98,08 г в 1 литре, будет иметь молярность 1 М и нормальность 2 Н. Это потому, что каждый 1 моль серной кислоты (h3SO4) содержит 2 моля атомов H +.
В таблице 1 перечислены молекулярные массы и эквивалентные массы важных кислот и оснований, используемых в винной лаборатории.
Приготовление 1 н. Раствора NaOH
Из приведенного выше обсуждения должно быть ясно, что для приготовления 1 нормального раствора нам необходимо знать эквивалент NaOH, который рассчитывается путем деления молекулярной массы на 1, то есть 40 разделенных на 1 = 40.Таким образом, эквивалентный вес NaOH равен 40. Чтобы приготовить 1 н. Раствор, растворите 40,00 г гидроксида натрия в воде, чтобы получить объем 1 литр. Для 0,1 н. Раствора (используемого для анализа вина) необходимо 4,00 г NaOH на литр.
Стандартизация
Перед тем, как мы начнем титровать этот образец вина, у нас есть еще один важный шаг — стандартизация раствора NaOH. Стандартизация — это просто способ проверить нашу работу и определить точную концентрацию нашего реагента NaOH (или другого). Возможно, наше разведение было неточным, или, может быть, весы не были откалиброваны, и в результате нормальность нашего раствора гидроксида натрия не равна точно 1 N, как мы предполагали.Так что нам нужно это проверить. Это достигается титрованием раствора NaOH кислотой известной силы (нормальность). Обычно для титрования основания используется 0,1 н. HCl. Реагент, 0,1 N раствор HCl, приобретается у поставщика химикатов, сертифицированного по концентрации. Это означает, что он был стандартизирован до известной концентрации. «Но разве это не ходит по кругу?» ты спрашиваешь. Нет, потому что кислоты стандартизированы до порошкообразной основы под названием KHP или гидрофталата калия. Его можно очень точно взвесить, потому что это мелкий порошок, а затем титруют кислотой.
Для стандартизации NaOH начните с пипетирования 10,0 мл 0,1 н. Соляной кислоты (HCl) в колбу. Добавьте примерно 50 мл воды (помните, что это не вода из-под крана) и три капли индикатора метилового красного. Заполните бюретку объемом 25 мл 0,1 н. Раствором гидроксида натрия и запишите начальный объем. Титруйте соляную кислоту до точки, при которой цвет становится лимонно-желтым и остается неизменным. Запишите окончательный объем.
Вычтите начальный объем из конечного, чтобы получить объем использованного NaOH, и подставьте его в уравнение ниже.
Нормальность NaOH = Объем HCl x Нормальность HCl
Объем использованного NaOH
Методы титрования
Прежде чем полностью освоить объемный анализ, нам необходимо обсудить некоторые методы титрования. Прежде всего осторожно обращайтесь с бюреткой. Избегайте повреждения узла наконечника и крана, поскольку повреждения и утечки в этих областях могут и будут влиять на производительность. Кроме того, обязательно записывайте окончательные и начальные значения объема точно, считывая нижнюю часть мениска раствора.Не пытайтесь втиснуть последний образец и опорожнить бюретку до самой нижней отметки; найдите время, чтобы правильно его пополнить. Чтобы облегчить чтение бюретки, возьмите белую учетную карточку и раскрасьте на ней черный квадрат, как показано. Держите его за шкалой бюретки при снятии показаний, чтобы лучше видеть мениск. По этой причине на некоторых бюретках действительно нарисована полоса.
Затем не забудьте перемешать образец во время титрования. Независимо от того, используете ли вы мешалку (рекомендуется) или перемешиваете, покручивая колбу вручную, раствор обязательно должен быть перемешан.Следите за тем, чтобы образец не выливался за пределы стакана / колбы и не позволял содержимому бюретки выпадать за пределы стакана. Кроме того, достаточно опустите бюретку, чтобы брызги образца не выходили из колбы во время титрования. Это не только плохая лабораторная практика, но также может быть опасным.
Безопасность — важный фактор при работе с бюретками, кислотами и щелочами. Осознайте, что вы имеете дело с агрессивными химикатами и хрупкой стеклянной посудой, относитесь к ней как к незаменимому вину в изысканном бокале.Это значит сознательно и с уважением. Надевайте как минимум защитные очки и лабораторный халат, также рекомендуются перчатки. Наполняя бюретку, выньте ее из подставки и держите под углом так, чтобы наконечник находился над раковиной. Таким образом, вся жидкость будет стекать в раковину, и вы сможете спокойно стоять на полу, а не на табурете. Опасно наклоняться над бюреткой, когда она стоит на столе.
Убедитесь, что у вас есть доступ к станции для промывания глаз или к чему-то, что может подавать струю воды к вашему телу и / или глазам в течение 15 минут — это рекомендованное OSHA средство для лечения попадания химических веществ в глаза и тело.Помните, что гидроксид натрия будет в бюретке на уровне глаз и выше, поэтому убедитесь, что ваше оборудование прикреплено к устойчивому основанию.
Надлежащая лабораторная практика может помочь вам более точно и эффективно контролировать качество ваших вин. Объемный анализ путем титрования — один из наиболее распространенных методов, используемых виноделом для анализа своего продукта. В постоянном поиске отличных вин важно совершенствовать свои навыки в этой области.
* Ранее опубликовано в Vineyard and Vintage View , Mountain Grove, MO.
Произошла ошибка при настройке пользовательского файла cookie
Этот сайт использует файлы cookie для повышения производительности. Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка вашего браузера для приема файлов cookie
Существует множество причин, по которым cookie не может быть установлен правильно. Ниже приведены наиболее частые причины:
- В вашем браузере отключены файлы cookie. Вам необходимо сбросить настройки своего браузера, чтобы он принимал файлы cookie, или чтобы спросить вас, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает вас, хотите ли вы принимать файлы cookie, и вы отказались. Чтобы принять файлы cookie с этого сайта, нажмите кнопку «Назад» и примите файлы cookie.
- Ваш браузер не поддерживает файлы cookie. Если вы подозреваете это, попробуйте другой браузер.
- Дата на вашем компьютере в прошлом. Если часы вашего компьютера показывают дату до 1 января 1970 г., браузер автоматически забудет файл cookie. Чтобы исправить это, установите правильное время и дату на своем компьютере.
- Вы установили приложение, которое отслеживает или блокирует установку файлов cookie. Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу. Чтобы предоставить доступ без файлов cookie потребует, чтобы сайт создавал новый сеанс для каждой посещаемой страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в cookie; никакая другая информация не фиксируется.
Как правило, в файлах cookie может храниться только информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта. Например, сайт не может определить ваше имя электронной почты, пока вы не введете его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступа к остальной части вашего компьютера, и только сайт, который создал файл cookie, может его прочитать.
О гидроксиде натрия — Tom’s of Maine
Что это?
Гидроксид натрия (NaOH) представляет собой белый воскообразный непрозрачный кристалл без запаха , состоящий из ионов натрия и гидроксид-ионов. Он также известен как щелок или каустическая сода и используется во многих отраслях промышленности для регулирования pH, для очистки питьевой воды, в бытовых чистящих средствах и в мыловарении.
Что он делает?
Это универсальный ингредиент, доступный в широком диапазоне классов и концентраций.На самом высоком уровне он очень едкий и может использоваться в качестве очистителя сточных вод, но при разбавлении он безопасен для работы и приготовления пищи.
В продуктах Tom’s разбавленные уровни гидроксида натрия используются для регулирования уровня pH в некоторых наших продуктах для ухода за полостью рта, что делается для повышения общей эффективности продукта. При растворении гидроксидная часть соединения реагирует с кислотами с образованием воды. Уровень pH регулируется (становится более щелочным), поскольку часть кислоты удаляется.
Это также ключевой ингредиент для приготовления многих особых блюд. Традиционное скандинавское блюдо лютефиск буквально переводится как «щелочная рыба», поскольку оно готовится из сушеного сига и щелока (общее название гидроксида натрия). Момини — это приготовление сушеных кукурузных зерен, восстановленных путем вымачивания их в растворе щелочи, а крендели с кренделями получают свою уникальную корочку из-за того, что их окунули в раствор щелочи перед выпечкой.
Как это сделано?
Наша модель управления помогает нам выбирать ингредиенты, которые были обработаны в соответствии с нашей философией здоровья человека и окружающей среды.
Гидроксид натрия получают из соленой воды (рассола). Чаще всего его получают путем электролиза рассола, солевого раствора (NaCl). Во время этого процесса вода (H 2 0) восстанавливается до газообразного водорода (H) и гидроксид-иона (OH). Ион гидроксида связывается с натрием с образованием гидроксида натрия (NaOH).
Какие есть альтернативы?
Существуют и другие более слабые соединения, которые могут буферизовать pH в формулах, но гидроксид натрия может использоваться в очень низкой концентрации и быть значительно эффективным.
Подходит ли мне этот вариант?
Гидроксид натрия в наших продуктах является пищевым и признан безопасным для общего использования в пищевых продуктах FDA 1 .


